Pr Patrick Fénichel abd, Dre Thérèse Greck cd
a Gynécologue/Endocrinologue CHU Nice, 170 chemin de l’Adret La Gaude 06610. Fenichel.p@chu-nice.fr
b Professeur émérite Université Côte d‘Azur
c Gynécologue/Endocrinologue Montpellier
d MEDEA Organisme de formation habilité à dispenser des actions labellisées DPC : Environnement et Périnatalité.
www.medea.fr
Résumé :
Des travaux épidémiologiques et expérimentaux de plus en plus nombreux suggèrent que l’environnement périconceptionnel maternel, voire paternel, joue un rôle déterminant sur l’état de santé à venir de l’enfant. Les polluants chimiques à activité de perturbateurs endocriniens en mimant, bloquant ou perturbant l’action des hormones sur le développement fœtal sont ainsi susceptibles via des modifications épigénétiques de favoriser la survenue de maladies chroniques. Réduire l’exposition fœtale en délivrant des conseils simples et pratiques à la future mère lors d’une consultation préconceptionnelle devrait par conséquent constituer un objectif prioritaire en médecine préventive périnatale.
Mots-clés : exposition maternelle ; micro-environnement fœtal, perturbateurs endocriniens, DOHAD, les 1000 jours, consultation préconceptionnelle
Introduction
L’examen attentif des registres de naissance dans les hôpitaux de zones industrielles britanniques plutôt défavorisées a permis, dans les années 80, à un épidémiologiste anglais, David Barker, de mettre en évidence une corrélation inverse très significative entre l’hypotrophie fœtale ou retard de croissance intra-utérin (identifiée par une réduction du poids de naissance normalisé pour l’âge gestationnel) et le risque de survenue, plusieurs décennies plus tard, de maladies métaboliques (obésité, diabète de type 2) et/ou de complications cardiovasculaires sévères (1). C’est l’environnement fœtal délétère (désordres nutritionnels et métaboliques de la mère, stress, tabac…) à l’origine de l’hypotrophie fœtale qui est responsable, via des modifications épigénétiques, du risque majoré à venir (figure 1 page 32).
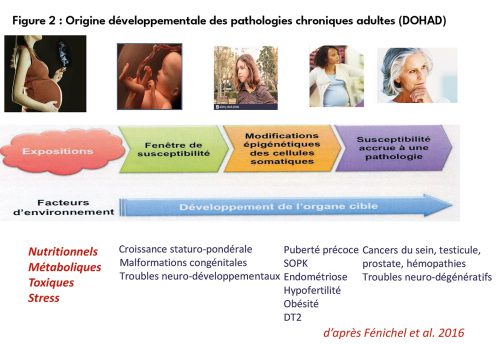
De nombreux travaux expérimentaux et épidémiologiques ont ensuite confirmé l’hypothèse de Barker conceptualisée sous le nom de DOHAD (Origine développementale des pathologies chroniques adultes) (2). Ainsi chez le rongeur, il a été montré qu’indépendamment de toute susceptibilité génétique, l’hyperglycémie ou la carence protidique maternelle est capable d’induire une obésité et/ou un diabète chez les descendants et que le stress maternel peut entrainer des troubles neurocomportementaux chez les petits, transmissibles sur plusieurs générations (3). Le suivi des enfants et petits-enfants des mères et grand-mères traitées pendant la première partie de leur grossesse par un estrogène de synthèse, le distilbène*, a confirmé que l’exposition fœtale à certaines molécules chimiques en dehors de tout effet mutagène pouvait se traduire dans l’espèce humaine par des malformations et par le développement de pathologies chroniques (4). L’importance de la qualité de l’environnement périnatal pour la santé à venir de l’enfant a été prise en compte par l’OMS dans ses recommandations et mise en avant il y a une dizaine d’années sous le vocable de la politique préventive dite des « 1000 jours », à savoir de la conception jusqu’à l’âge de 2 ans (5), et plus récemment par les autorités sanitaires françaises.
Les perturbateurs endocriniens environnementaux (PEEs)
Parmi ces facteurs environnementaux, certains polluants chimiques perturbateurs endocriniens sont susceptibles du fait de leur affinité pour différents récepteurs nucléaires (récepteurs aux estrogènes, androgènes, hormones
thyroïdiennes ou autres récepteurs nucléaires) d’interférer avec les hormones physiologiques indispensables au développement fœtal (6). La spécificité des perturbateurs endocriniens par rapport à d’autres polluants chimiques est d’agir comme une hormone à très faibles doses de l’ordre du nanogramme ou du picogramme par millilitre. Ils peuvent être reprotoxiques, voire tératogènes ou carcinogènes, mais ne sont généralement pas mutagènes. Ils agissent plutôt par des modifications épigénétiques théoriquement réversibles. Les modifications épigénétiques ainsi induites ont été impliquées dans l’augmentation du risque de survenue de nombreuses affections chroniques (malformations génitales, autisme, hyperactivité et troubles de l’attention, asthme, allergies, obésité, diabète, endométriose, stérilité, cancers pédiatriques et adultes…) (6).
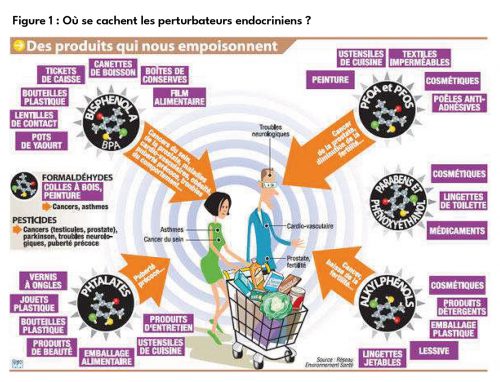
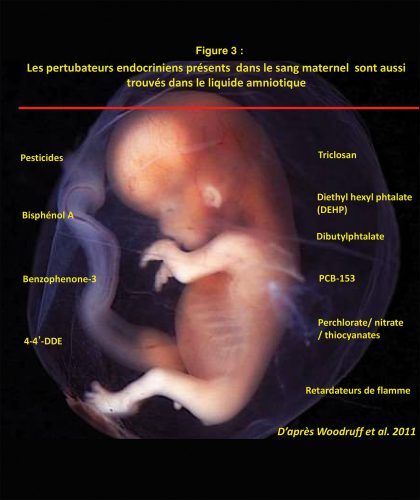
Ces molécules chimiques, le plus souvent de synthèse, sont présentes dans l’environnement domestique quotidien (figure 2 page 33). Elles peuvent être issues de l’industrie (plastifiants comme les bisphénols et les phtalates, solvants, détergents, bactéricides, retardateurs de flamme, imperméabilisants, antiadhésifs, déchets industriels) ou de l’agriculture (pesticides). L’exposition se fait par voie aérienne, cutanée et surtout orale via l’alimentation (additifs alimentaires, métaux lourds comme le plomb, l’arsenic, le mercure ou le cadmium). Ces substances le plus souvent lipophiles se bio-accumulent dans les tissus graisseux d’où elles sont libérées avec les acides gras dans la circulation, traversent chez la femme enceinte le placenta et sont retrouvées dans le sang du cordon, le liquide amniotique (figure 3 page 33), la plupart des organes fœtaux, et le lait maternel (7,8). Réduire l’exposition de la mère, et donc du fœtus et du nourrisson par des mesures préventives simples, constitue par conséquent un challenge auquel les équipes périnatales sont aujourd’hui confrontées.
Pourquoi réduire l’exposition maternelle dès la période préconceptionnelle ?
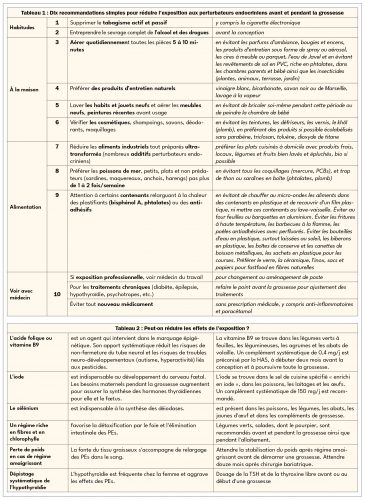
La première consultation prénatale a lieu souvent tardivement vis-à-vis des recommandations que l’on peut proposer pour réduire l’exposition maternelle et les risques fœtaux. D’où l’intérêt de développer le principe d’une consultation préconceptionnelle afin d’agir suffisamment tôt, y compris vis-à-vis de l’exposition environnementale (9). Ces informations et ces conseils préventifs pourraient être prodigués aussi bien par des sages-femmes, des gynécologues, des médecins généralistes ou des pédiatres, pour peu qu’ils soient formés. Une enquête récente menée à Marseille auprès des professionnels de la périnatalité (10) et une enquête nationale menée auprès des médecins généralistes dans le cadre d’une thèse de médecine soutenue à Nice (11) ont montré que les soignants souvent interrogés sur les perturbateurs endocriniens avaient toutefois des difficultés à apporter une réponse éclairée. Des conseils préventifs concernant l’exposition aux polluants chimiques perturbateurs endocriniens ont fait l’objet d’une mise au point par l’Endocrine Society (12) et l’International Federation of Gynecology and Obstetrics (FIGO) dès 2015 (13). Les tableaux 1 et 2 page 34 montrent ceux que nous proposons depuis 2016 (6) avec comme objectif : simplicité, efficacité et une certaine validité scientifique malgré les difficultés inhérentes à l’épidémiologie environnementale.
Comment réduire l’exposition maternelle aux PEEs ?
Exposition professionnelle
Certaines personnes sont plus exposées professionnellement aux pesticides, produits d’entretien, solvants et produits chimiques. Une consultation avec le médecin du travail est à prévoir dès le désir de grossesse pour évaluer les risques d’exposition au travail. Un aménagement du poste de travail peut être nécessaire. Le lieu d’habitation proche de zones exposées (viticulture, agriculture intensive, zone industrielle…) doit être pris en considération.
Sevrage alcool, tabac, drogues
Pendant la grossesse, les effets délétères du tabac sont connus, mais il faut insister surtout sur le tabagisme passif et la présence dans les goudrons du tabac d’hydrocarbures aromatiques polycycliques (PAH), de cadmium, de benzopyrène et autres PEEs. Les effets de programmation fœtale de ces perturbateurs endocriniens ont été largement démontrés chez le rongeur et confirmés par des données épidémiologiques chez l’humain (14).
L’origine des aliments
On préfèrera cuisiner les produits locaux que d’utiliser des produits cuisinés ultra-transformés contenant de nombreux additifs chimiques. En période périconceptionnelle, on favorisera les produits issus de l’agriculture biologique et raisonnée pour les fruits et légumes, mais aussi pour les produits laitiers, les œufs et la viande. Une telle attitude a déjà été évaluée dans des études prospectives sur des milliers de couples mère/enfant avec une diminution significative de l’HTA gravidique, de malformations génitales (15), d’obésité infantile et d’allergies (16). De nombreux PEEs sont des polluants organiques persistants (POP) qui se bio-accumulent dans les graisses et les nappes phréatiques, et sont rémanents. Ils sont présents dans l’environnement des années après leur interdiction comme le DDT estrogénique et son dérivé très stable le DDE anti-androgénique. Il est conseillé de toute façon de laver abondamment les légumes et les fruits, de consommer beaucoup de légumes verts et de fibres qui accélèrent l’élimination des POPs présents dans les viandes et les poissons (17).
Le mode de cuisson et la conservation des aliments
Il est déconseillé vivement de cuisiner ou réchauffer des aliments dans des contenants en plastique ou recouverts par un film alimentaire plastique, car ils contiennent du bisphénol A dont les sous-unités sont relarguées par hydrolyse. Certaines poêles antiadhésives ont dans leur revêtement des composés perfluorés toxiques ; il est préférable d’utiliser des poêles ou des casseroles en acier inoxydable, fonte, fer ou de cuisiner dans la porcelaine. À fortes températures, la cuisson dans des contenants en cuivre ou en aluminium (dont le papier aluminium) entraine un passage du métal dans les aliments. La friture est déconseillée, car à haute température l’huile dégage de l’acrylamide toxique pour le cerveau fœtal (18). Attention aussi aux boîtes de conserve et aux canettes dont la paroi interne est recouverte d’un film plastique ; il est conseillé d’utiliser des bouteilles et contenants en verre. Attention également à l’eau du robinet en cas de canalisations anciennes et/ou tuyaux en plomb.
La consommation de poissons
Les poissons sont certes une source d’oméga-3, d’iode et de sélénium, mais de nombreux polluants/PEs comme les PCBs, le cadmium et le mercure se bio-accumulent dans la graisse des poissons. Depuis 2013, la directive de l’Ansess (19) recommande chez la femme enceinte la consommation de poissons maigres, plats et non prédateurs comme le maquereau, le hareng, la sardine et l’anchois, pas plus de deux fois par semaine, interdit les coquillages, les poissons gras ou d’eau douce. Attention aux boîtes de conserve de thon riches en plomb. La recommandation raisonnée de l’Ansess est encore peu connue des soignants. Outre les poissons, les oméga-3 se trouvent également dans l’huile de colza, les légumes verts et les fruits à coque. L’iode se trouve aussi dans le sel de table spécifié « enrichi en iode », dans les laitages et les œufs. Le sélénium indispensable à la désiodase, utilisée par le fœtus pour transformer la thyroxine (T4) maternelle en triiodothyronine (T3), se trouve également dans les légumes, les abats et les jaunes d’œuf.
Produits cosmétiques
Il est important pendant la période périconceptionnelle de modifier l’utilisation de certains cosmétiques : coloration capillaire, défrisant, khôl ou rouge à lèvres (plomb), maquillage, déodorant, shampoing, savon. Il faut privilégier les cosmétiques sans triclosan, parabènes, toluène, ou dioxyde de titane ni huiles essentielles. Il faut utiliser des produits plus naturels, écolabellisés, lire les étiquettes et utiliser des applications spécifiques de contrôle des composants.
Produits d’intérieur, de jardin, bricolage, vêtements
Éviter les pesticides, herbicides, insecticides, les produits contenant toluène (solvant) ou n-hexane. Pour le jardinage ou le bricolage, on utilise des produits « bio » et on se protège (gants, masque). Pour la chambre du bébé et des parents, le choix des matériaux est important : opter pour des produits écolabellisés. Éviter les sols en PVC, source de phtalates et favorisant la survenue d’asthme (20), et les meubles en contreplaqué. Se méfier des retardateurs de flamme polybromés souvent présents dans les tentures, rideaux, moquettes, jouets et des perfluorés antitaches et imperméabilisants présents dans les textiles. Aérer la pièce et laisser les meubles neufs dans un endroit ventilé avant usage pour éliminer les toxiques. Laver les habits neufs, draps, serviettes avant premier usage pour éliminer les retardateurs de flammes, imperméabilisants et antifroissages.
L’air intérieur
Les études récentes sur la qualité de l’air intérieur montrent que c’est la source principale d’exposition aux polluants chimiques. Lors de la préparation de la chambre de bébé, ils sont la principale source d’exposition materno-fœtale avec des effets secondaires : petit poids de naissance, avortement spontané, retard de croissance, malformations, trouble du neurodéveloppement, asthme. Les détergents, les solvants contiennent du trichloroéthylène, du tétrafluoroéthylène, du formaldéhyde, du benzène, du toluène, du styrène et des phtalates (di-2-éthylhéxyle et le diisobutyle) (21). Il est donc important d’aérer les pièces très régulièrement au moins dix minutes par jour, ventiler pendant les travaux, privilégier les matériaux écolabellisés et des produits d’entretien naturels.
Les médicaments
Tout traitement chronique doit être réévalué en cas de désir de grossesse.
Pendant la grossesse, pas d’automédication, la prise d’antalgiques, d’aspirine, d’anti-inflammatoire est à risque. Même le paracétamol est un toxique PE. Pendant la grossesse, il faut le prescrire à la dose la plus faible et pour une durée la plus courte (22).
Comment réduire les effets de l’exposition fœtale ?
L’acide folique ou vitamine B9
L’alimentation est souvent pauvre en vitamine B9, insuffisance majorée par une surconsommation de thé et de café. Le manque d’apport en B9 peut influencer le niveau de méthylation de l’ADN, une des marques épigénétiques (23). On sait que la vitamine B9 réduit le risque de non-fermeture du tube neural. Aussi, il est recommandé un apport de vitamine B9 en début de grossesse (9). Récemment, il a été démontré que l’apport de vitamine B9 réduit le risque de survenue de troubles du spectre autistique, de troubles cognitifs, de syndrome d’hyperactivité avec déficit de l’attention lors d’exposition aux pesticides organochlorés ou organophosphorés. Cet effet de la vitamine B9 est obtenu avec des doses égales ou supérieures à 0,8 mg/j (24). Si la supplémentation d’acide folique avant et pendant la grossesse est essentielle, une enquête française de périnatalité en 2010 (25) montrait néanmoins que moins de 25 % des femmes enceintes avaient pris de l’acide folique dès le début de leur grossesse. L’apport d’acide folique doit débuter deux mois avant la conception à 0,4 mg/j, voire 0,8 mg en cas de risque majoré (antécédents d’anomalies, épilepsie, diabète, exposition critique aux pesticides) et poursuivi pendant toute la grossesse.
L’apport iodé
L’iode est primordial pour la synthèse des hormones thyroïdiennes et pour le développement du cerveau fœtal. Au cours du premier trimestre, le fœtus est dépendant de la thyroxine (T4) maternelle qui traverse le placenta et se transforme en triiodothyronine (T3) grâce à une désiodase (métalloenzyme au sélénium). À partir du deuxième trimestre, le fœtus commence à synthétiser ses hormones à partir de l’iode maternel après passage placentaire. Au cours de la grossesse, la femme a des besoins en iode qui augmentent par passage vers le fœtus, augmentation de la clairance rénale et augmentation de la synthèse des hormones thyroïdiennes maternelles (26). Une étude montre que 75 % des femmes enceintes dans la région de Nice ont une carence modérée en iode malgré la proximité de la mer (27). La supplémentation par 150 μg/j d’iode est impérative avant la conception. À ce complément, il est nécessaire d’ajouter dans son assiette du sel attesté enrichi en iode (à ne pas utiliser pour la cuisson, l’iode étant volatile), d’arrêter le tabac (28), et de réduire l’exposition aux PEEs.
Éviter les cures d’amaigrissement sévères avant conception
Bien que l’obésité soit associée à des risques majorés de diabète gestationnel, d’hypertension gravidique, de complications obstétricales et de risques métaboliques chez le futur enfant (29), il n’est pas souhaitable de démarrer une grossesse tout de suite après un amaigrissement important et rapide. En effet, les POPs très lipophiles et stockés dans le tissu adipeux vont être relargués dans la circulation sanguine comme cela a été très bien montré après chirurgie bariatrique chez des jeunes femmes en âge de procréer (30). Ainsi, après chirurgie bariatrique est-il préconisé d’attendre 18 mois au mieux sous contraception avant d’envisager une grossesse, ce temps permettant en outre de substituer correctement les carences vitaminiques induites par le montage digestif (30).
Conclusion
Nous sommes tous exposés quotidiennement à de nombreux polluants chimiques, dont certains exercent une activité de perturbateurs endocriniens.
Les périodes fœtale, périnatale et prépubertaire sont des fenêtres critiques où l’exposition prolongée ou cumulée aux PEs est susceptible d’entrainer des modifications épigénétiques qui constituent des facteurs de risque de survenue de différentes maladies chroniques pouvant se développer de la naissance à l’âge adulte. L’information prodiguée par les soignants est aujourd’hui primordiale. Cette information préconceptionnelle vient en complément de l’adaptation des thérapeutiques, du dépistage des situations à risque, de mesures préventives de type vaccinale ou nutritionnelle. Elle doit être simple, compréhensible, argumentée, pratique, mais non stigmatisante à délivrer à tous les couples dans l’optique de réduire l’exposition aux perturbateurs endocriniens et, par conséquent, diminuer les risques associés.
Références bibliographiques
[1] Barker DJ, Osmond C, Golding J, Kuh D, Wadsworth ME. Growth in utero, blood pressure in childhood and adult life, and mortality from cardiovascular disease BMJ. 1989; 298:564-572.
[2] Charles MA, Delpierre C, Bréant B. Developmental origin of health and adult diseases (DOHaD): evolution of a concept over three decades. Med Sci (Paris). 2016; 32:15-20.
[3] Gapp K, von Ziegler L, Tweedie-Cullen RY, Mansuy IM. Early life epigenetic programming and transmission of stress-induced traits in mammals: how and when can environmental factors influence traits and their transgenerational inheritance? Bioassays. 2014; 36:491-502.
[4] Fenichel P, Brucker-Davis F, Chevalier N. The History of Distilbène (Diethylstilboestrol)* Told to Grandchildren – The Transgenerational Effect. Annales d’endocrinologie. 2015 ;76:253-262.
[5] Fleming TP, Watkins AJ, Velazquez MA, et al. Origins of lifetime health around time of conception: causes and consequences. Lancet 2018; 391:1842-1852
[6] Fénichel P, Brucker-Davis F, Chevalier N. Endocrine disruptors, reproduction and hormone-dependent cancers. Presse Médicale 2016; 45 :63-72
[7] Brucker-Davis F, Wagner-Mahler K, Delattre I, et al. Cryptorchidism Study Group from Nice Area Cryptorchidism at birth in Nice area (France) is associated with higher prenatal exposure to PCBs and DDE, as assessed by colostrum concentrations.Hum Reprod. 2008; 8 :1708-18
[8] Fini JB, Mughal BB, Le Mével S, et al. Human amniotic fluid contaminants alter thyroid hormone signalling and early brain development in Xenopus embryos. Sci Rep. 2017; 7 :43786-97.
[9] HAS 2009 « projet de grossesse: informations, messages de prévention, examens à proposer » www.has-santé.fr
[10] Sunyach C, Antonelli B, Tardieu S, Marcot M, Perrin J, Bretelle F. Environmental Health in Perinatal and Early Childhood: Awareness, Representation, Knowledge and Practice of Southern France Perinatal Health Professionals. Int J Environ Res Public Health. 2018; 5:2259-75
[11] Cardin AS. Élaboration d’un guide de conseils préventifs contre les risques liés aux perturbateurs endocriniens à l’usage des médecins généralistes. Thèse de Médecine soutenue à Nice 29 Sept 2016 https://dumas.ccsd.cnrs.fr/dumas-01407770/document
[12] Diamanti-Kandarakis E., Bourguignon J.P., Giudice L.C., et al. Endocrine-disrupting chemicals: an Endocrine Society scientific statement Endocr Rev, 2009,30: 293-342
[13] Di Renzo et al. International Federation of Gynecology and Obstetrics opinion on reproductive health impacts of exposure to toxic environmental chemicals. Int J Gynaecol Obstet. 2015; 131 :219-25.
[14] Dechanet C, Anahory T, Mathieu Daude JC et al.. Effects of cigarette smoking on reproduction. Hum Reprod Update. 2011,17:76-95
[15] Torjusen H, Brantsæter AL, Haugen M, et al. Reduced risk of pre-eclampsia with organic vegetable consumption: results from the prospective Norwegian Mother and Child Cohort Study. BMJ Open. 2014, 10; 4, e006143.
[16] Mie A, Andersen HR, Gunnarsson S, et al. Human health implications of organic food and organic agriculture: a comprehensive review. Environ Health. 2017; 16:111
[17] Jin W, Otake M, Eguchi A, et al.. Dietary Habits and Cooking Methods Could Reduce Avoidable Exposure to PCBs in Maternal and Cord Sera. Sci Rep. 2017,1:17357- 71.
[18] El-Sayyad HI, Abou-Egla MH, El-Sayyad FI, El-Ghawet HA, Gaur RL, Fernando A, Raj MH, Ouhtit A. Effects of fried ppotato chip supplementation on mouse pregnancy and fetal development. Nutrition 2011;27:343-50.
[19] ANSSES Saisine n° 2012 – SA – 0202
[20] Shu H, Jönsson BA, Larsson M, Nånberg E, Bornehag CG. PVC flooring at home and development of asthma among young children in Sweden, a 10-year follow-up. Indoor Air. 2014 ;24:227-35.
[21] Triquet J. L’exposition pré-natale aux polluants de l’air intérieur et les stratégies d’information de la femme enceinte. Mémoire de L’Ecole des Hautes Etudes en santé Publique 2011
[22] Mazaud-Guittot S, Nicolas Nicolaz C, Desdoits-Lethimonier C, et al. Paracetamol, aspirin, and indomethacin induce endocrine disturbances in the human fetal testis capable of interfering with testicular descent.J Clin Endocrinol Metab. 2013; 98: E1757-67.
[23] Dolinoy D.C., Huang D., Jirtle R.L. Maternal nutrient supplementation counteracts bisphenol A-induced DNA hypomethylation in early development. Proc Nat Acad Sci U S A, 2007; 104: 13056-13061
[24] Schmidt RJ, Kogan V, Shelton JF, Delwiche L, Hansen RL, Ozonoff S, Ma CC, McCanlies EC, Bennett DH, Hertz-Picciotto I, Tancredi DJ, Volk HE. Combined Prenatal Pesticide Exposure and Folic Acid Intake in Relation to Autism Spectrum Disorder. Environ Health Perspect. 2017 ; 125:097007.
[25] Blondel B, Kermarrec M. Enquête nationale périnatale 2010. 2011. http://drees.social-sante.gouv.fr/etudes statistiques/publications/recueils-ouvrages-et- rapports/rapports/article/les-naissances-en-2010-et-leur-evolution-en-2003.
[26] Brucker-Davis F, Hiéronimus S, Fénichel P. Thyroid and the environment. Presse Med. 2016; 45:78-87
[27] Hiéronimus S, Bec-Roche M, Ferrari P, Chevalier N, Fénichel P, Brucker-Davis F. [Iodine status and thyroid function of 330 pregnant women from Nice area assessed during the second part of pregnancy]. Ann Endocrinol (Paris). 2009 ; 70: 218-24-32.
[28] Brucker-Davis F, Ganier-Chauliac F, Gal J, et al. Neurotoxicant exposure during pregnancy is a confounder for assessment of iodine supplementation on neurodevelopment outcome. Neurotoxicol Teratol. 2015;51:45-51
[29] Mission JF, Marshall NE, Caughey AB. Pregnancy risks associated with obesity Obstet Gynecol Clin North Am. 2015; 42:335-53.
[30] Fénichel P, Coquillard P, Brucker-Davis F, et al. Sustained bloodstream release of persistent organic pollutants induced by extensive weight loss after bariatric surgery: Implications for women of childbearing age. Environ Int. 2021; 151:106400.


